
日立は1950年代からX線や超音波を使った画像診断装置の開発など,医療・ヘルスケアの進歩に貢献してきた。
その中で,研究開発グループは主に機器やシステムを革新する先端技術やアプリケーションの開発を担う。
2000年代には,陽子線がん治療システムを開発し,世界有数の医療機関への納入を実現。
近年は,診断機器や治療システムにITやAIを導入し,患者一人ひとりのQoL向上に資するとともに,社会全体の「医療費削減」と「医療の質の向上」への貢献をめざす。
今後はさらに,医療データベースの構築や利活用のためのアプリケーション開発など,ITやデータサイエンスを活用した臨床判断サポートや疾病予防分野にも取り組んでいく。
北海道大学病院粒子線がん治療装置
[1]陽子線治療システムの全体構成 シンクロトロンで加速した陽子を治療室に輸送し,照射野形成装置によって腫瘍形状に成形して照射する。
シンクロトロンで加速した陽子を治療室に輸送し,照射野形成装置によって腫瘍形状に成形して照射する。
[2]動体追跡スポットスキャニングシステム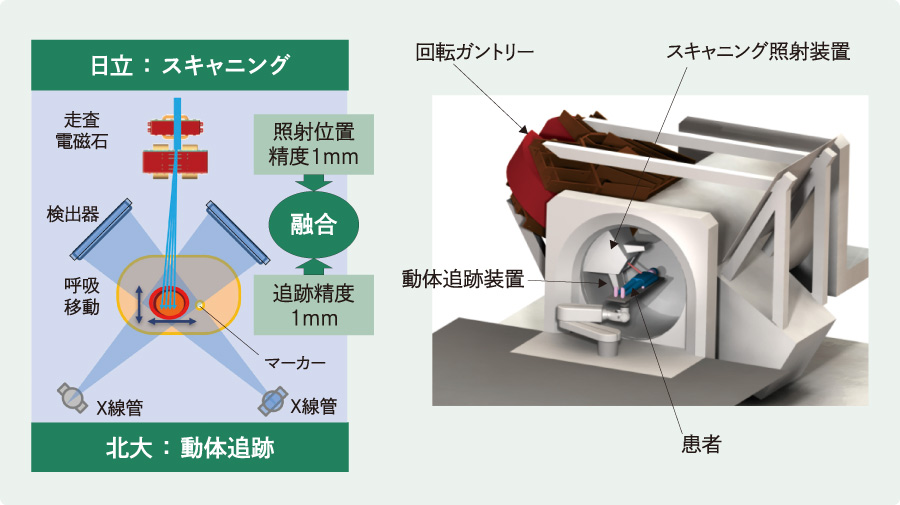 患者に対して,2方向からのX線透視画像撮像系を備える。腫瘍近傍に刺入した金マーカーをX線透視画像で捉え,検出器(FPD)上の金マーカー位置を基に幾何学的に金マーカーの三次元位置を把握する。金マーカーの位置検出を高精度(±1mm以内)で把握し,臓器の移動を追跡することが可能となっている。
患者に対して,2方向からのX線透視画像撮像系を備える。腫瘍近傍に刺入した金マーカーをX線透視画像で捉え,検出器(FPD)上の金マーカー位置を基に幾何学的に金マーカーの三次元位置を把握する。金マーカーの位置検出を高精度(±1mm以内)で把握し,臓器の移動を追跡することが可能となっている。
2017年5月,日立と国立大学法人北海道大学が共同で開発した「動体追跡粒子線がん治療装置」が,公益社団法人発明協会の全国発明表彰「恩賜発明賞」を受賞した。これは,全国発明表彰で最も優れた発明に贈られるもので,科学技術の向上および産業の発展に寄与することを目的に1926年に創設された権威ある賞である。
粒子線がん治療は,放射線によるがん治療法の一つで,水素の原子核である陽子や炭素イオンなどの粒子を加速器で光速の70%程度まで加速し,生成した粒子線を腫瘍に集中して照射するというもの([1]参照)。粒子線は,加速された粒子のエネルギーで決まる深さで線量が最大(ブラッグピーク)になり,体内に進入した直後に線量が最大となる従来のX線による治療に比べて,患部にピンポイントで照射できるという特長がある。そのため周囲の正常細胞への影響を極力抑えることができ,治療に伴う痛みもなく,患者のQoL(Quality of Life)を維持しながらがん治療ができるために大きな期待が寄せられているのだ。
装置開発が始まった1980年代後半から頭頸部や前立腺で成果を上げ,現在では日本人に多い肝臓がん・肺がんの治療や,小児がんの治療にも適用されている。
今回の受賞理由は,肺や肝臓のように呼吸などによって移動する患部に対して,腫瘍位置をリアルタイムに捉えて正確に粒子線を照射する技術を開発し,副作用などによる患者への負担をより軽減したことである。これを可能にしたのが,日立が世界に先駆けて開発したスポットスキャニング照射技術と,北大が持つ動体追跡照射技術の両者を搭載した融合システムだ([2]参照)。2009年に国家プロジェクト「最先端研究開発支援プログラム(FIRST)」に採択され,5年の歳月をかけて実現した成果で,北大では2014年からこのシステムを採用した陽子線によるがん治療が行われている。
 平本 和夫
平本 和夫
研究開発グループ 技師長
1978年入社,原子炉の設計研究を経て現在,粒子線治療システムの研究開発に従事。工学博士。
陽子線がん治療装置の開発の歴史は,1980年代後半まで遡る。米国ロマリンダ大学で陽子線による治療専用装置が設置されたのを機に,国内でも粒子線の医療への応用をめざす国家プロジェクトが始まった。日立は,1950年代から物理研究に用いられる大型加速器プロジェクトへの参画や工業用の加速器の製造・開発で培ってきた技術を活かし,1988年には独立行政法人放射線医科学総合研究所の重粒子線治療システムプロジェクトに参画。システムの心臓部となるシンクロトロン加速器(円形加速器の一種)などの設計・製作を担当した。
その後,2000年には福井県 財団法人若狭湾エネルギー研究センターに,陽子線がん治療や物理,化学,生物学,農学など幅広い先端分野の研究開発に利用される多目的シンクロトロン加速器システムを,2001年には筑波大学附属病院 陽子線医学利用研究センターに陽子線治療システムをそれぞれ納入するなど,日本におけるこの分野の技術開発を牽引することになった。
黎明期から研究に携わり,現在まで陽子線がん治療システムの開発に従事する研究開発グループ技師長の平本和夫は次のように当時を振り返る。
「最初は本当に事業になるのかという意見もありましたが,私自身は日立の技術的優位を確信していました。他社と競合するなかで日立が採用されたのは,陽子線の出射位置を自在に制御できる『高周波駆動ビーム出射法』などを開発し,医療用装置に必要とされる精度にまで技術を高めることができたからだと思います。また,日立グループには加速器の駆動に不可欠な電磁石などの周辺の要素技術があったことに加え,高精度な制御装置に仕立て上げる部隊がいたことも大きな強みでした」
高周波駆動ビーム出射法は平本自身による発明だ。四極電磁石の磁場強度を適切に設定して,安定限界(収束も発散もしない状態)を一定に保ったまま出射のために陽子線に加える高周波のオン/オフで出射の開始,停止を150μsという短時間で切り替える画期的な方法である。これにより,陽子線の照射を高精度にコントロールできるようになった。
[3]MDアンダーソンがんセンター陽子線治療施設の回転ガントリー治療室および散乱体照射法とスキャニング照射法の装置構成比較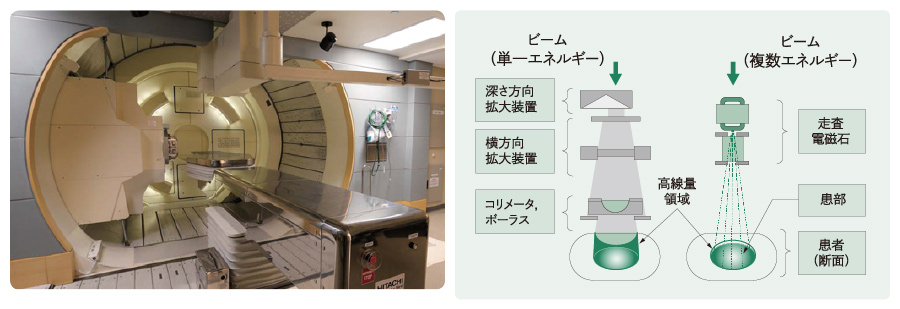 散乱体照射法(図左)は,横および深さ方向に広げたビームを横方向患部形状に切り出す。スキャニング照射法(図右)は,電磁石と加速器でビームを三次元的に走査する。
散乱体照射法(図左)は,横および深さ方向に広げたビームを横方向患部形状に切り出す。スキャニング照射法(図右)は,電磁石と加速器でビームを三次元的に走査する。
こうした実績は,海外にも知れ渡ることとなる。米国テキサス州にある世界トップクラスのがん専門病院であるMDアンダーソンがんセンター(MD Anderson Cancer Center:MDA)が日立の技術に興味を示し,他社との競合の末,2002年に治療室4室からなるシステムの設計,製作の受注に漕ぎ着けた。2006年から3治療室の稼働を開始し,2008年には,世界初となるスポットスキャニング照射技術を用いる4番目の治療室の稼働を開始した([3]参照)。
スポットスキャニング照射技術とは,加速器から輸送された細い陽子線の径をできるだけ拡大させずに照射し,その照射位置を腫瘍の形状に合わせて点を打つように精密に走査するというもの。従来の二重散乱体方式に比べて複雑な形状のがんにも高精度で陽子線を照射でき,これまで腫瘍の形状に合わせて個別につくる必要があった器具(コリメータ,ボーラス)も不要となるうえ,陽子線の利用効率も高いという特長がある。
2007年にFDA(米国食品医薬品局)許可を取得して,MDAへの納入後,米国の医療施設を中心に導入を検討したいという相談が相次ぎ,以後,名古屋陽子線治療センター(2008年),米メイヨー・クリニック(2011年),米セント・ジュード小児研究病院(2012年),米シブリー・メモリアル病院(2015年),香港養和病院,シンガポール国立がんセンター(2016年),スペインナバラ大学病院(2017年)など,世界の医学界をリードする医療機関への受注が続いている([4]参照)。
「それまで陽子線がん治療システムの受注は他社との競合で苦難の連続でしたが,MDAに世界初となるスポットスキャニング照射方式の機器を納入したことで,海外市場への普及が一気に進みました。欧米トップ企業との競争は大変厳しいものがありますが,これらの経験を重ねる中,世界でも十分に戦えるという手応えを感じています」(平本)
もう一つ,冒頭で紹介した北大との協創で日立が実現したのが,機器の小型化である。スポットスキャニング照射方式では陽子線の利用効率が高いことから,加速・出射可能な陽子線量を低減できるとして,機器の構成を見直し,偏向電磁石と四極電磁石の機能を結合させるなどして小型化を図った([5]参照)。
「『最先端研究開発支援プログラム(FIRST)』がスタートした途端,政策の影響などで予算が半減して大変苦労しましたが,それが結果として小型で安価な製品の開発に結びつき,その後の普及につながりました。2016年には,北大と共同で治療直前に患者の体内の状態を三次元で正確に撮像して,より高精度な位置決めを実現する回転ガントリー搭載型コーンビームCTシステムを開発し,臨床使用を始めています。今後の医療機器としての本格普及を見据えて,小型化および複合化はますます重要になってくるでしょう。
世界トップの医療機関へのシステムの納入から多くを学び医工連携を実現し,いまや日立には開発・設計,営業など,多彩な人材からなる最強のチームが存在します。最近では,システムを納入,または納入予定のユーザーを招き,ユーザーミーティングを開催して,性能や操作性の一層の向上を図っています。今後はさらに,ITやAI(Artificial Intelligence)の活用でケアサイクルを革新するシステムを開発し,グローバルトップをめざしていきます」(平本)
 小池 麻子
小池 麻子
未来投資本部 ヘルスケアナショナル
プラットフォームプロジェクトリーダ
1994年入社,ヘルスケアイノベーションセンタ センタ長を経て現在ヘルスケアITの新規事業立上げに従事。理学博士。東北大学客員教授併任。
現在,医療・ヘルスケアで最も重視されるのが,「医療費削減」と「医療の質の向上」の二つである。米国では,公的保険,民間保険ともに従来の出来高払い(fee for service)から, アウトカムや医療の質に応じた保険償還(value based payment)に変わりつつある。先述の陽子線がん治療システムは,医療の質の向上に資する先端技術の一つだが,今後のさらなる普及は,治療の効果と医療費のバランスがカギを握ることになるだろう。
一方,国内の医療費は41.3兆円(2016年度)と高水準で,うち国庫負担は14兆円にも上る。2025年には5人に1人が75歳以上となる超高齢化社会を迎えることから,医療費削減は官民が一体となって取り組むべき喫緊の国民的課題である。
東北大学メディカルメガバンクなどのゲノム解析システム構築などに従事するとともに,東京大学医学系大学院・附属病院や大学共同利用機関法人 情報・システム研究機構 国立遺伝学研究所などと国家プロジェクト等で疾患関連変異の探索および疾患関連変異の体系化・データベース化に従事してきた,未来投資本部ヘルスケアナショナルプラットフォームプロジェクトリーダの小池麻子は,今後の医療費削減のポイントを次のように語る。
「医療費削減は,保険者の支払いと院内コストの2種の削減がありますが,前者は予防,治療,予後の最適化で患者のトータルコストを下げる必要があり,後者を実現するには,検査時間短縮による人件費の低減や診断スループット向上が不可欠でしょう。つまり,検査・計測の自動化,診断の定量化が求められているわけです。これらは同時に医療の質の向上にも貢献します。
日立は1950年代からX線や超音波を使った画像診断機器,さらには1970年代から生化学自動分析装置などの体外診断機器の開発を手がけ,長年,精度向上に努めてきました。今後は機器の精度を上げるだけでなく,二つの課題解決のために,ITおよびAIを取り入れて,過去の大量の検査データを学習し,これまで人間が判断していたことを自動化していく必要があります」
[7]QPMで合成できる多彩な診断画像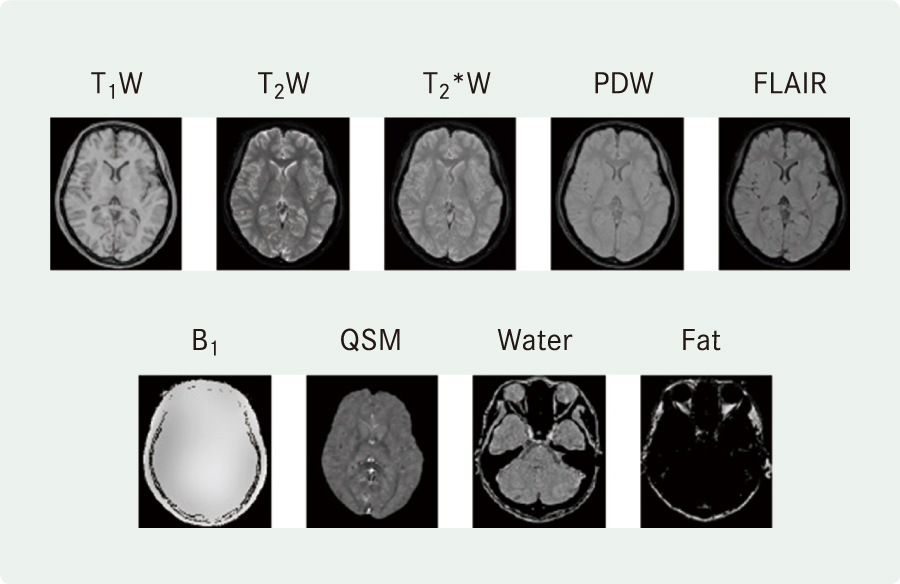 QPMで得られた複数組織物理量定量画像から,定量的磁化率画像(QSM)を含む各種診断画像を一度に合成する技術を開発している。
QPMで得られた複数組織物理量定量画像から,定量的磁化率画像(QSM)を含む各種診断画像を一度に合成する技術を開発している。
[8]DKIの概要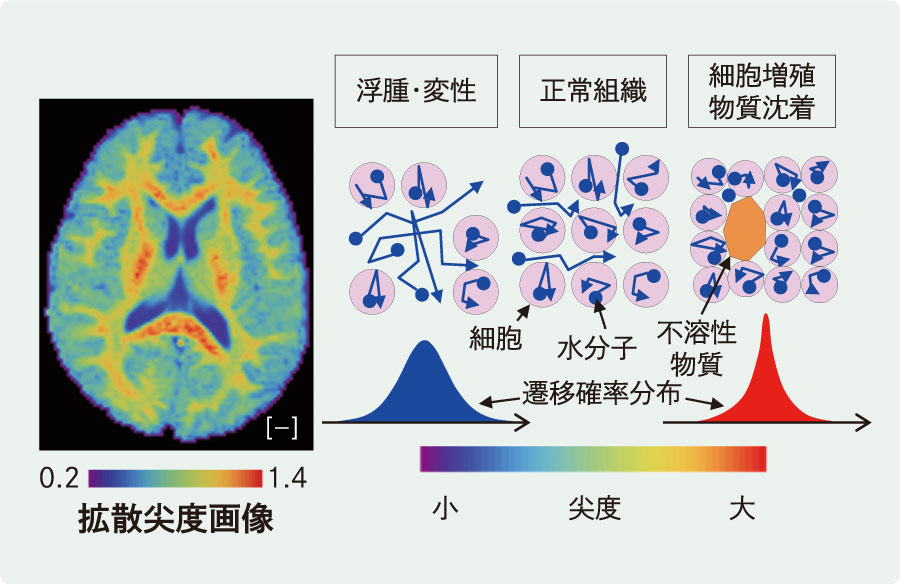 拡散尖度画像の例を示す。脳神経変性疾患の早期診断をめざし,疾患初期の微小な構造の変化を捉える技術を開発している。
拡散尖度画像の例を示す。脳神経変性疾患の早期診断をめざし,疾患初期の微小な構造の変化を捉える技術を開発している。
そこで現在,日立は超音波診断装置を中心に自動化を進めている。超音波診断装置は,非侵襲で安全性が高く,リアルタイムに身体の断面画像が得られる装置であり,1960年に日本無線医理学研究所(後のアロカ)が世界で初めて製品化して以来,小型で安価,可搬性も高いことから医療のさまざまな領域で活用されていて,自動化への期待も高い。
特に産婦人科の重要な検査の一つに,超音波診断装置による胎児の体重計測がある。これまでは,操作の煩雑さや胎児の動きに妨げられて,検査時間の長大化や検査者による値のばらつきが問題となってきた。これらの問題を解消するために,日立は断面画像を選択した後,胎児の体重を自動計測するシステムをAIの活用により開発,ARIETTA 850に搭載して好評を得ている([6]参照)。
「循環器の検査では,大量の検査結果の学習により撮像断面の高精細な自動判別を実現し,負荷心エコーのワンボタン計測を可能にして,計測時間を1/4〜1/5に短縮しました。また,肝疾患の診断に用いられる組織の硬さ(繊維化)の違いを画像化する肝臓向けのエラストグラフィ(Elastography)技術を開発,2015年に製品化しています。今後は,偽陽性が多いがん診断分野などにも超音波による自動診断の技術を展開していく予定です」(小池)
一方,生体に多量に含まれる水素原子核の核磁気共鳴現象を利用して生体組織の性質を画像化するMRI(Magnetic Resonance Imaging:磁気共鳴撮影法)では,診断を定量化する技術を追究している。生体機能や病変の定量的評価を可能にするために,撮影シミュレータで数値的に作成した輝度関数を用いて各種組織物理量を分離する高速定量画像化技術(fast Quantitative Parameter Mapping:QPM)を開発。1回の撮像で得られた三次元データから輝度関数を使って複数の組織物理量定量画像を作成することで,これまでMRI検査で用いられてきた各種強調画像を合成でき,検査時間も1/3程度に削減できるようになった([7]参照)。
同時に,QPMで定量的磁化率画像(Quantitative Susceptibility Mapping:QSM)も生成できる。磁化率を定量的に評価することで,出血や石灰化などをそれぞれ異なる輝度で描出できるため,脳虚血疾患や腫瘍の診断において重要な役割を果たすと期待されている。
現在,これらの定量化技術については,国立研究開発法人日本医療研究開発機構(AMED)の実証事業として,診断が難しいとされる軽度認知障害(MCI)と初期のアルツハイマー型認知症の診断において,北海道大学病院と共同で評価を実施しているところだ。
「特に脳疾患は患者のQoLに大きく関わるため,早期診断が重要です。そうしたことから研究開発グループは,MRIの診断アプリケーションとして拡散尖度イメージング(Diffusion Kurtosis Imaging:DKI)の開発も進めています。これは水分子の拡散運動が組織構造によって制限される度合いを遷移確率密度分布の尖度(kurtosis)によって評価するというものです。現在,岩手医科大学と共同で行っているパーキンソン症候群鑑別の臨床研究で検証しています([8]参照)。
こうした一連の技術により,定量的な画像が得られれば,AIを使った病変の自動診断にも役立ちます。しかもこれらの技術は原理的にメーカーの機種に依存しないことからすべてのMRIに搭載可能であり,将来は疾患画像のデータベース化が進み,自動診断が加速していくことになるでしょう」と小池は語る。
[9]次世代大型免疫自動分析装置e801(左)および複合型生化学自動分析装置3500(右) 業界最高となる検査速度(左)と3種の検査の1台への集約(右)を通じ,検査結果の迅速な報告と臨床検査業務の効率化を実現する。
業界最高となる検査速度(左)と3種の検査の1台への集約(右)を通じ,検査結果の迅速な報告と臨床検査業務の効率化を実現する。
[10]次世代DNAシーケンサー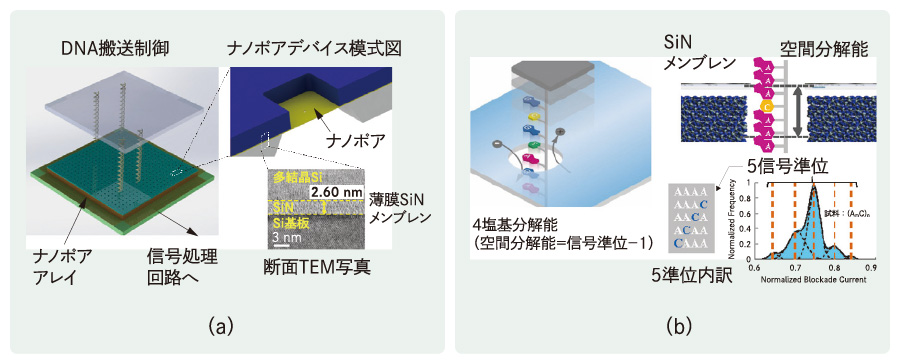 DNA一分子の塩基配列を読み取る技術を開発している。(a)開発中のアレイ型ナノポアデバイスとデバイス部拡大図,(b)試作ナノポアデバイスを用いて確認した4塩基空間分解能を示す。
DNA一分子の塩基配列を読み取る技術を開発している。(a)開発中のアレイ型ナノポアデバイスとデバイス部拡大図,(b)試作ナノポアデバイスを用いて確認した4塩基空間分解能を示す。
一方,体外診断用医療機器に関しても,検査の完全自動化や早期診断のための感度向上を加速させている。
日立ハイテクノロジーズが開発・販売する免疫自動分析装置および生化学自動分析装置は,Roche Diagnosticsとの協業により現在,世界シェア1位である。2016年6月には,15年ぶりに次世代大型免疫装置e801を市場投入した。最大搭載項目数を48項目に拡張し,冷蔵機能,試薬開閉機能を改良したことにより搭載試薬の安定性を改善するとともに校正間隔を大幅に延ばした。研究開発グループはフローセルの流路設計,送液機構の安定化などに貢献し,従来機と同等の床面積で従来比1.75倍の毎時300テストを実現した。
また,同社では検体検査結果の迅速な報告と臨床検査業務の効率化をめざして複合型の自動分析装置3500を開発。従来の透過光による生化学的検査項目に加え,抗原物質に特異な抗体をコーティングしたラテックス粒子を用いた高感度の免疫分析と血液凝固検査項目測定を一台にまとめて,10分程度での結果の出力を実現した。今後は,がんマーカなどの項目を増やしていく予定だ([9]参照)。
「もう一つ,日立がこれまで脈々と培ってきた技術に,DNAシーケンサーがあります。かつて神原秀記名誉フェローが開発したキャピラリーアレイ型DNAシーケンサーはヒトゲノムの解読に大きく貢献しましたが,現在は一分子レベルでリアルタイムに塩基配列を読み取る次世代装置の開発が進められています。研究開発グループでは近年,半導体材料中に形成したナノサイズの穴にDNAを通し,その際のイオン電流の変化で塩基配列を読み出すソリッド・ナノポア型シーケンサーを開発し,世界に先駆けて一分子で4塩基種を識別できるようになりました([10]参照)。
また,がんの遺伝子解析は,従来の組織生検ではなく,簡単に採取できる末梢血の血中循環腫瘍DNA(circulatory tumor DNA:ctDNA)の測定による早期発見や個人に最適な治療選択,再発・予後の予測に期待が集まっています。ctDNAの変異測定は微量のため困難ですが,最近,digital droplet PCR技術の開発により,微量な変異も測定できるようになりつつあります。今後の研究開発に期待してください」と小池は展望を語る。
 長我部 信行
長我部 信行
ヘルスケアビジネスユニット
CSO/CTO
1980年入社,電子顕微鏡の開発,応用研究に従事し,2001年基礎研究所所長,2011年中央研究所所長を経て2014年より現職。理学博士。
ここまで見てきたように,これまで日立が連綿と培ってきた医療・ヘルスケア関連の技術はいまや,ITやAIと結びつくことで,医療費削減と医療の質の向上という二つを実現し,ケアサイクル全体を革新しつつある。今後の医療・ヘルスケアの展望について,ヘルスケアビジネスユニットCSO/CTOの長我部信行は次のように語る。
「日立では,例えば悪性脳腫の治療のためのオープンMRIを開発し,術中のMRI画像を確認しながら手術ができるシステムを開発し,東京女子医科大学をはじめとする主要な大学病院の脳神経外科へ納入しています。今後はさらに,診断・治療機器をIoT(Internet of Things)でつなぎ,診断と治療を一体化することで,ヘルスケアサイクルのスループットの向上を実現していきたいと考えています」
もう一つ,今後の医療で重要なポイントとなるのが,各個人に最適な精密医療(Precision Medicine)だと長我部は強調する。これは,オバマ前米国大統領が一般教書演説の中で“Precision Medicine Initiative”を発表して以来,脚光を浴びる考え方だ。
「がんの遺伝子変異の解析から,その人に合った治療薬・治療法の選択をすることもその一つです。さらには,がんの再発防止や予後・ケアのために手術と放射線治療,抗がん剤治療などを併用するケースが増えていますが,その際に,さまざまな情報から個人に最適な予防や治療法を選択できるような取り組みが求められているのです。そのためには,データベースやAIの活用が欠かせません」(長我部)
日立には1980年代から医療データベースの構築に取り組んできた歴史があり,最近では,AIを活用して電子化された診断結果とレセプト(診療報酬明細書)から,個人の健康状態や医療費の予測モデルの構築を手がけている。その一例として,米国ユタ大学との共同研究で,ユタ大学が有する糖尿病患者の電子カルテデータとクレイムデータを機械学習で解析し,糖尿病治療薬の効果を予測,比較する技術を開発した。これにより,患者ごとに治療効果が高く,医療費も低減すると予想される薬の選定の支援につなげようとしている。今後はさらに予測モデルから健康指導を行い,疾病を予防することで医療費削減に貢献していく([11]参照)。
「現在,政府は医療データの統合と利活用の推進を進めており,レセプトデータや電子カルテデータなどを信頼のおける代理機関において匿名加工して,産業活用や医療の質の向上に利用していこうとしています。そのITインフラ構築にわれわれも参画しています。
今後は,ヘルスケアサイクルの革新だけでなく,それぞれの分野を融合し,特に公共や金融部門とも連携しながら,IoT時代における社会システムの全体の再構築に注力していきたい。そのためには,医工連携はもとより,さまざまな異分野のパートナーや顧客との協創をさらに進めていく考えです」と,長我部は締めくくった。
[11]日立グループのヘルスケア事業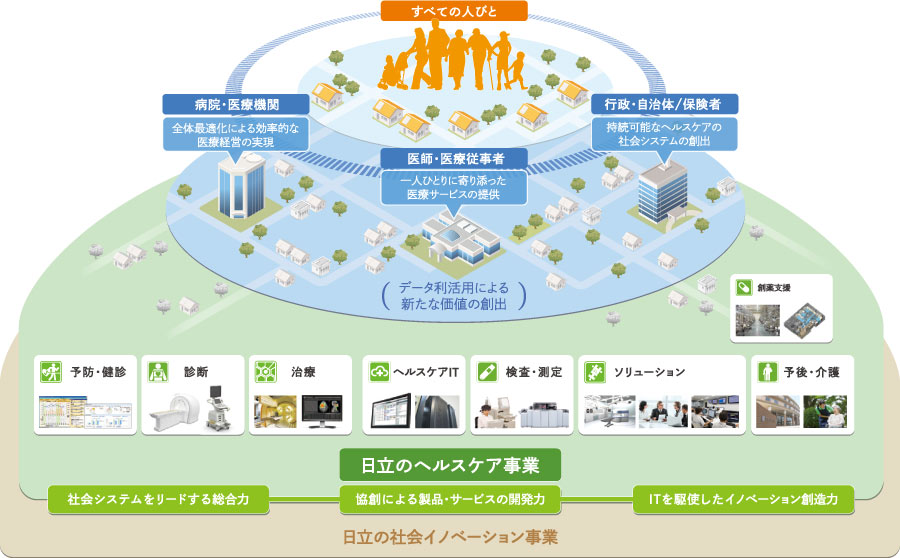 医療事業の実績と幅広い分野で培ってきた技術の下,多種多様なパートナーとの協創を通じて,生涯にわたって一人ひとりに最適なヘルスケアサービスと,世界各国の事情に適した持続可能な社会システムの実現に貢献していく。
医療事業の実績と幅広い分野で培ってきた技術の下,多種多様なパートナーとの協創を通じて,生涯にわたって一人ひとりに最適なヘルスケアサービスと,世界各国の事情に適した持続可能な社会システムの実現に貢献していく。