株式会社日立ハイテクノロジーズと,ストックホルムに本社を構えるヴィロノヴァ社(Vironova AB)は,製薬・生命科学分野における新たなバイオ医薬品の効率的な開発に貢献することをめざしている。ここでは,日立ハイテクノロジーズの機器・システムとヴィロノヴァ社の画像解析・自動化技術を組み合わせた,医療分野のニーズに応える協創事例を紹介する。







株式会社日立ハイテクノロジーズと,スウェーデンのストックホルムに本社を構えるヴィロノヴァ社(Vironova AB)は,両社の中核を担う技術を組み合わせ,製薬・生命科学分野における新たなバイオ医薬品の効率的な開発への貢献をめざしている。
ヴィロノヴァ社は製薬業界向けの電子顕微鏡メーカーであり,TEM(Transmission Electron Microscope:透過型電子顕微鏡)の制御を行う独自のソフトウェア開発を手掛けている。中でも同社が特化しているのは,顕微鏡操作の自動化と,AI(Artificial Intelligence)やマシンラーニングを活用した革新的な画像解析である。
規制の厳しい生物製剤開発の分野において使用される電子顕微鏡には,客観的かつ自動化された画像解析が必要不可欠である。
ここでは,日立ハイテクノロジーズの機器・システムとヴィロノヴァ社の自動化ソフトウェアを組み合わせ,高まり続ける医療分野のニーズに応える協創事例を紹介する。
増え続ける人口と高齢化の進行という問題を抱える現代社会において,人類はがんや認知症といった疾患,人の往来によって引き起こされる集団感染,複数の抗生物質に対して耐性を有する細菌系統の拡散といった脅威に直面している。しかし一方で,生体物質を治療薬として用いるバイオ医薬品の登場など,製剤開発の分野では革命が起きつつある。
生物学的製剤に使用される生体由来の物質には,遺伝子,組み換え抗体,核酸などの生体分子がある。これらに共通するのは,従来使用されていた化学物質よりもはるかに大きな分子の物質という点である。電子顕微鏡は,こうした物質の特性を直接的かつ詳細に分析することができる。
最先端の生物医学研究を代表する存在である生物製剤は,代替医療のない疾患の治療に効果が期待されており,現代の医薬品開発の主流となりつつある。一部の生物製剤や遺伝子治療の成功例は,既に大きな注目を集めている。
ヴィロノヴァ社は遺伝子治療分野の研究開発に精通しており,日立ハイテクノロジーズとの最初の協創プロジェクトでは,バイオ医薬品開発における分析のボトルネックを解消するソリューションのデモンストレーションが行われた。
2017年,数十年に渡る研究の末に,米国初の遺伝子治療薬がFDA(Food and Drug Administration)に認可された。FDAはこれらの製品を生物製剤と規定し,販売開始から12年間の独占販売権を付与した。
そのうちの一つは,2017年8月に承認されたノバルティス社のKymriah※1)(tisagenlecleucel)であり,小児を含む若年層の急性リンパ芽球性白血病(ALL:Acute Lymphoblastic Leukemia)の治療薬として期待されている。また2017年10月には,Gilead Sciences Inc.のリンパ腫治療薬Yescarta※2)(axicabtagene ciloleucel)が承認されている。これらの治療薬は,キメラ抗原受容体発現T細胞(CAR-T:Chimeric Antigen Receptor-T)を用いた養子免疫療法の例である。
CAR-T細胞を用いた治療は,遺伝子治療と免疫療法の組み合わせである。まず,患者から取り出したT細胞と呼ばれる免疫細胞に遺伝子操作を行い,がん細胞を認識するキメラ抗原受容体(CAR)を発現させる。その後,細胞を患者の血流内に戻すと,遺伝子操作されたT細胞ががん細胞を攻撃するという仕組みである。CAR-Tを用いた臨床試験が成功した例は多数あり,今後,幅広い血液がんや固形腫瘍の治療への適用が期待されている。米国臨床腫瘍学会(ASCO:American Society of Clinical Oncology)は「Clinical Cancer Advances 2018」の中で,がん治療の分野における2018年で最も重要な進歩として,CAR-Tの名前を挙げている。
遺伝子治療の臨床試験対象となる疾患のうち,大多数の65%を占めるがんに次いで大きな比率を占めるのが,単一遺伝子疾患(11.1%)である。欠損または損傷した遺伝子を補うことで遺伝性遺伝子障害の治療を試みる遺伝子治療は,この分野ではユニークな治療法である2)。
2017年後半,Spark Therapeutics社のLuxturna※3)が成人・小児を対象とした眼の遺伝性疾患の治療薬として承認された。これは網膜内の細胞にウイルスベクターを注入する遺伝子治療によって遺伝子を正常な状態に修復し,視覚を回復させるものである。
このほか,今日までに約2,600件の臨床試験を経て,6種類の遺伝子治療薬が多くの国々で認可されている2),3)。こうした流れを受けて市場からの投資は増加しており,自社の遺伝子治療関連製品の製造と商業化をめざす企業は活気づいている。
遺伝子治療はまさに,新たな医療パラダイムの代表例である。しかし一方では,患者や医師の元に届く前段階,すなわち開発・製造段階での課題も多い。
遺伝子治療を患者に適用する際は,極めて厳格な安全ガイドラインに準拠する必要がある。そのため,遺伝子治療関連製品に適した分析機器の開発が強く求められている。2004年,FDAはバイオ医薬品製造において,PAT(Process Analytical Technology:工程分析技術)を導入した。目的は,従来の限定的な製品検査に代わる,製造プロセス全体を通じた徹底的な分析と,広範な最終製品試験の重要性を示すことである。これに伴い,各製薬関連企業は重要品質特性を計測し,より分かりやすく,コントロールしやすい製造プロセスを実現するための新たな分析技術の研究を開始している2)。
遺伝子治療では,遺伝子の異常を補ったり,有益なタンパク質を生成したりといった目的で,遺伝物質を細胞の中に導入する。一部の遺伝子治療では,遺伝子を運ぶためのキャリア(ベクター)として,ウイルスが利用される。これらのウイルスは感染症を引き起こさないよう遺伝子操作を加えられており,患者の細胞に感染することで新しい遺伝子を導入することができる。
あらゆる遺伝子療法において重要な役割を果たすベクターには,一般的にレンチウイルス(LV:Lentivirus),アデノウイルス(AV:Adenoviridae),アデノ随伴ウイルス(AAV:Adeno-associated Virus)が用いられる。一方でウイルスベクターの特性評価と品質管理において課題となっているのが,ウイルスの構造の複雑さである。最も単純な組み換えウイルスベクターである組み換えアデノ随伴ウイルス(rAAV:Recombinant Adenovirus-associated Virus)であっても,その構造の複雑さは組み換えタンパク質をはるかに凌ぐ。
大規模かつ最適なウイルスベクターの開発に際しては,製品の安全性,品質,均質性,および有効性を確保するため,品質特性を監視する正確で再現性の高い分析ツールが重要となる。
遺伝子療法用ウイルスベクターの製造においてモニタリングすべき重要品質特性とは,すなわち,ウイルスの効力,種別,数,純度,凝集,指定遺伝子が組み込まれていない空のエンプティーウイルス(Empty Virus)の数,タンパク質含有量,そして製品の安全性である。これに対し,現在ではさまざまな特性評価方法が存在するが,どの方法を適用するかは発現系と同じくウイルスの種別に依る。
生体物質は複雑で繊細な混合物であり,精製,特性評価および分析が容易でなく,一般的にその取り扱いは難しいとされる。これらの物質は凝集しやすく,壊れやすく,また汚染されやすい。
これらの物質の発見から量産化,品質管理のためのロバストなプロセスの開発を経て,医薬製品へと至る道程は複雑である。その過程には,純度(図1,図2参照)や完全性(図3参照)など,良質な製品を生産するために監視・制御すべきパラメータが数多く存在する。こうした監視・制御の面においては,電子顕微鏡が大いに活躍する。
図1|TEMを用いた試料観察 アデノ随伴ウイルス中の汚染をTEM(Transmission Electron Microscope)にて観察した画像の例を示す。
アデノ随伴ウイルス中の汚染をTEM(Transmission Electron Microscope)にて観察した画像の例を示す。
図2|一次粒子と不純物を区別する形態学的分類による自動純度分析 アデノウイルス粒子と不純物の面積比を表す,2つの試料の純度計測の結果を示している。
アデノウイルス粒子と不純物の面積比を表す,2つの試料の純度計測の結果を示している。
図3|壊れたカプシド構造を持つ粒子を特定するnsTEM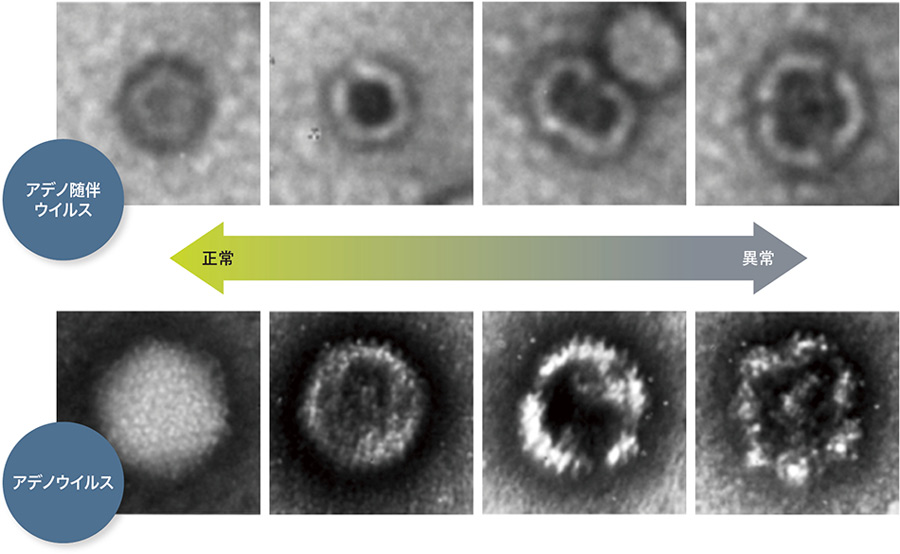 汚染されたアデノ随伴ウイルス試料のTEM分析(nsTEM:Negative Stain TEM)は,壊れたカプシド構造を持つ粒子を特定する再現性の高い手法である。壊れた粒子は中心部が暗く見えるため,特定が可能である。
汚染されたアデノ随伴ウイルス試料のTEM分析(nsTEM:Negative Stain TEM)は,壊れたカプシド構造を持つ粒子を特定する再現性の高い手法である。壊れた粒子は中心部が暗く見えるため,特定が可能である。
複雑な生体システムを調査するうえで最も有力なツールの一つが,電子顕微鏡によるイメージングである。電子顕微鏡によって得られる画像と数値は,製剤工程の監視で現在利用されている間接法では得ることができない,意義深いデータである。
しかしながら,製薬産業において電子顕微鏡を適切にレンダリングするには,処理と分析の自動化が求められる。これによってロバスト性,ばらつき低減,高い再現性,高スループットが実現できる。有益な分析データを素早く得ることで,迅速かつより適切な判断が可能となり,処理を早期に最適化することが可能となる。
ヴィロノヴァ社の強みは顕微鏡操作の自動化と,AIやマシンラーニングを活用した革新的な画像分析であり,これは,デジタルテクノロジーの適用によって製造効率を向上させるIndustrie 4.0と呼ばれる大きな流れの,製薬産業における一例と言える4)。
日立ハイテクノロジーズの120 kV透過電子顕微鏡HT7800シリーズと,ヴィロノヴァ社の自動化ソフトウェアを用いて実施された最初のフィージビリティスタディでは,ファージセラピーと呼ばれる新しい遺伝子治療法の研究を通じて,遺伝子治療におけるウイルス分析の在り方が示された。
バクテリアウイルス(バクテリオファージ,または単にファージとも言う。)を用いて細菌感染症の治療を行うファージセラピーは,過去1世紀近くにわたって実施されてきたが,近年,抗生物質の有効性が低下していることに伴い,改めて関心が寄せられている5)。
共同研究の結果,試料の品質に関する詳細なデータが得られたほか,顕微鏡を操作するうえでのいくつかの重要なステップを自動化することに成功し,検査に必要な時間が飛躍的に短縮された。例えばビームアライメントの所要時間は,通常の10%にまで短縮することができた。
さらに,サンプルグリッドのスクリーニングが自動化されたことで,サンプル分析時のオペレータの負担も大きく軽減された(図4,図5参照)。加えて最も重要な成果として,バクテリオファージの重要品質特性を確認し,ばらつきを定量化する画像解析による定量データ取得を実現した。
遺伝子治療,生物製剤は,ともに生産プロトコールの確立が初期段階にある若い分野である。患者の安全に関わるパラメータに対する見解は未だ変化を続けており,この分野のニーズは多様である。今後多くのプロジェクトが臨床段階に移行し,製造業者が大規模な生産プロセスを開発すると,さらなる課題が表出してくることが予想される。
製品品質と患者の安全を確保する処理を最適化することは容易ではない。成功のカギは信頼性の高い分析ソリューションから得られるデータである。精細な試料の画像を取得可能な日立ハイテクノロジーズのTEMと,画像から試料の品質を反映した正確な数値データを生成可能なヴィロノヴァ社の自動画像解析プラットフォームの融合は,電子顕微鏡というフィジカルな世界とサイバー技術を融合させた好事例である。日立ハイテクノロジーズとVironova ABは,こうした新たな治療法に求められる安全・安心な製品の生産を支えるべく,今後も研究開発を続けていく。