製薬分野の品質管理向上に寄与する微生物迅速検査装置Lumione BL-2000
ハイライト
医薬品の微生物汚染を防止するため,製品や製造環境の微生物管理は必須である。しかし,従来の微生物検査法は所要時間が数日以上に及ぶという課題があった。特に再生医療で用いられる細胞製剤などは,生細胞を含むために滅菌処理ができず使用期限が短いことなどから,微生物検査迅速化へのニーズが今までになく高まっている。
日立はATP生物発光法により高感度に菌を検出する微生物迅速検査装置Lumione BL-2000を開発し,製薬用水や低分子・高分子医薬品の微生物検査の迅速化を実現した。
本稿では,さらにATP法の適用を広げるべく実施中の製造環境および細胞製剤の無菌検査の迅速化技術開発について紹介する。

1. はじめに
医薬品製造においては患者の安全確保のため,原材料から製品の製造・加工,出荷まですべての過程で医薬品の汚染を防止し,一定の品質を保証しなければならない。医薬品の主な汚染リスクの一つには微生物汚染が挙げられ,微生物は重要な管理項目の一つとなっている。そのため微生物検査は,原料,中間体,最終製品,製薬用水および製造環境のそれぞれの工程において実施されている。
微生物検査の対象である細菌および真菌(以下,「菌」と記す。)のサイズは1~10 μm程度であり,光学顕微鏡で試料中から少数の菌を検出するのは難しい。そこで従来は培地に試料を添加して培養し,菌を増殖させてから目視で検出する培養法による検査が実施されており,菌数検査では寒天培地を用いて数日,無菌試験では液体培地を用いて14日の培養時間が必要と定められている1),2)。この従来法に代わって微生物迅速検査法を導入することで,より早い微生物検出による医薬品の品質管理向上,および検査結果待ち時間の短縮による製造・出荷の迅速化と製造コスト低減が期待される。特に,近年発展が著しい再生医療に用いられる細胞製剤は,生きたヒト細胞(以下,「細胞」と記す。)を含むことから加熱滅菌処理などができず,また使用期限が数日である場合が多いため,最終製品の微生物検査の迅速化は急務となっている3)。レギュレーションにおいても,2016年の第十七改正日本薬局方(以下,「局方」と記す。)に微生物迅速検査法が収載され,また,2019年に厚生労働省より発出された「再生医療等製品の無菌製造法に関する指針」にて微生物迅速検査法の検討が要求されるなど4),今後,微生物迅速検査法が普及していくと予想される。
日立は,医薬品製造における微生物管理の強化,それによる患者のQoL(Quality of Life)向上に貢献する製品として微生物迅速検査装置Lumione BL-2000(以下,「Lumione」と記す。)を開発した。本検査システムは,ATP(Adenosine Triphosphate:アデノシン三リン酸)生物発光法(以下,「ATP法」と記す。)を用いた高感度な菌検出により微生物検査の迅速化を実現している5)。
2. ATP法を用いた微生物迅速検査の概要
ATPは,すべての生物細胞が代謝過程でエネルギーを供給するために利用している化合物であり,菌にも含まれる。ATP法は,ホタルの発光原理として発見された発光効率の高いルシフェリン―ルシフェラーゼ反応を用い,ATP量を発光計測により定量する方法である。従来のATP法の検出下限は100 amol(1 amol= 10-18 mol)程度であった。
日立のLumioneは,専用試薬(前処理試薬,発光試薬)および微弱な発光を検出可能な発光計測装置の開発により,ATP検出下限0.3 amolという高感度検出を実現した。菌1 CFU(Colony Forming Unit:寒天培養法により計数した生菌数)当たりのATP量(以下,「菌のATP内包量」と記す。)は多くの菌種において1 amol程度かそれ以上なので,本検査システムは菌1 CFU程度に相当するATPが検出できるという点で画期的である。
Lumioneの計測手順を図1に示す。試料の前処理工程ではまず,試料を孔径0.45 μmのフィルタで濾過することでフィルタ上に菌を濃縮し,かつ液体試料は濾液として除去する。次にフィルタ上で菌体外ATP消去反応を行い,その後,菌体内ATPを少量の抽出試薬で抽出することで濃度の高い菌ATP試料を得て,菌の検出感度を向上している。また,試薬の工夫により,芽胞からもATP抽出が可能となっている。得られたATP試料の入った計測チューブ,および発光試薬をLumioneにセットし計測を行う。Lumione内では自動で,計測チューブを1本ずつ順番に発光計測部へ搬送し,発光試薬分注,および発光計測を行う。計測チューブは同時に24本までセット可能で,計測時間は1本当たり5分,24本で2時間となっている。
医薬品製造におけるLumioneの適用事例として,製薬用水および低分子・高分子医薬品から試料前処理工程を含み最短1時間で指標菌1 CFUを検出可能であることをすでに報告している5)。製薬用水設備の立ち上げ期間短縮による生産設備の稼働率向上や,医薬品の出荷迅速化により,製造コスト低減が期待できる。日立は,さらにさまざまな微生物検査の迅速化ニーズに対応するべく,検査プロトコルの開発を進めている。
次章からは,環境検査および細胞製剤の無菌試験の迅速化に向けて開発中の技術を紹介する。
図1|Lumioneの計測手順 試料を濾過してフィルタ上で菌を濃縮し,前処理を行うことで高感度化している。前処理の所要時間は約1時間である。Lumioneでは計測チューブ1本ずつに対し,自動で発光試薬分注および発光計測を行う。同時に24本までセット可能で,測定時間は1本当たり5分,24本で2時間である。
試料を濾過してフィルタ上で菌を濃縮し,前処理を行うことで高感度化している。前処理の所要時間は約1時間である。Lumioneでは計測チューブ1本ずつに対し,自動で発光試薬分注および発光計測を行う。同時に24本までセット可能で,測定時間は1本当たり5分,24本で2時間である。
3. 環境検査への適用例
医薬品の製造環境の微生物管理では,空中浮遊菌,落下菌,表面付着菌のモニタリングが実施される。特に注射剤などの無菌製剤を製造する無菌操作区域は,無菌管理されている。
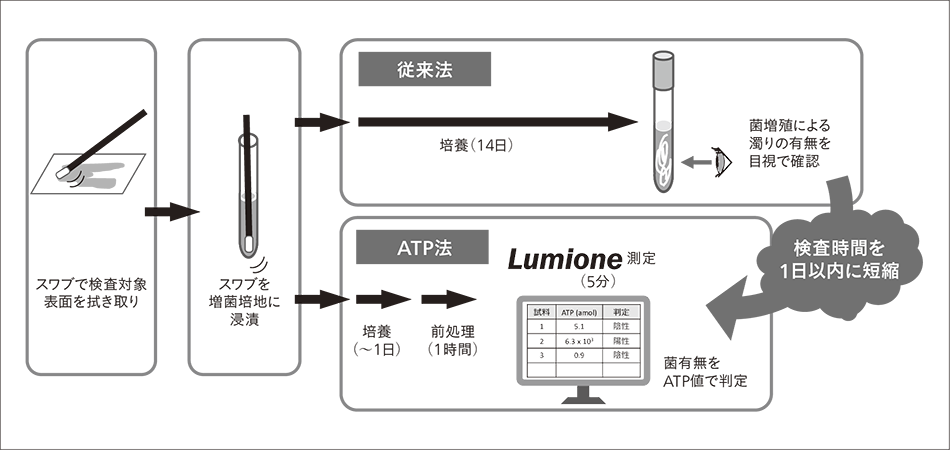
そこで表面拭き取りによる無菌試験を想定した検査手順の一例を図2に示す。従来法では,市販のスワブ(綿棒状の検体採取用具)で検査対象表面を拭き取ってから液体培地にスワブを浸漬して増菌培養し,14日後に菌増殖による濁りがないことを目視で確認することで無菌と判定する。一方,ATP法を用いる場合,短時間の培養後にLumioneでの前処理および計測を行い,ATP計測値があらかじめ定めた閾値以下であることで無菌と判定する。目視で菌を検出するには107 CFU程度まで菌が増殖する必要があるのに対し,ATP法はより少ない菌数を検出可能であるため,培養時間を短くすることができる。培養時間は,試料自体が持つATPによる計測阻害の程度,菌のATP内包量,および増殖速度から決定される。
そこで無菌操作を行う作業員の表面付着菌の無菌試験にATP法を適用することを想定し,検討を行った結果を表1に示す。市販のクリーンルーム用資材(滅菌済みニトリル手袋および滅菌済みポリプロピレン腕カバー)を試料とし,10 cm×10 cmの面を市販スワブで拭き取って資材自体が持つATP量を計測したところ,ATP量は1 amol未満であり,菌検出閾値を1 amol程度に設定可能であることが確認された。また,作業員から混入しやすく増殖の遅い菌として知られるCutibacterium acnes(C. acnes:アクネ菌,DSM 1897)15 CFU,および無菌試験手法の適合性を試験する際に使用するよう局方に指定されている菌種のうちでATP内包量が最も小さいPseudomonas aeruginosa(P. aeruginosa:緑膿菌,ATCC 9027)21 CFUをスワブに添加し,4時間の培養後にATP計測を行った。その結果,ATP法による菌検出が可能であった。
今後は1日以内の無菌試験実用化をめざし,実際の製造環境の表面拭き取りや各種環境菌でのデータを蓄積して検査プロトコルを確立していく。
表1|表面拭き取り試験の測定例 市販のクリーンルーム用滅菌済み手袋および腕カバーを拭き取ったスワブのATP量は1 amol未満であり,菌検出に影響しないことが確認された。また,C. acnesおよびP. aeruginosaの計測値から,初菌数1 CFUでも4時間の培養により菌ATPは数amolとなり,ATPによる検出が可能と考えられる。
市販のクリーンルーム用滅菌済み手袋および腕カバーを拭き取ったスワブのATP量は1 amol未満であり,菌検出に影響しないことが確認された。また,C. acnesおよびP. aeruginosaの計測値から,初菌数1 CFUでも4時間の培養により菌ATPは数amolとなり,ATPによる検出が可能と考えられる。
4. 細胞製剤の無菌試験への適用例
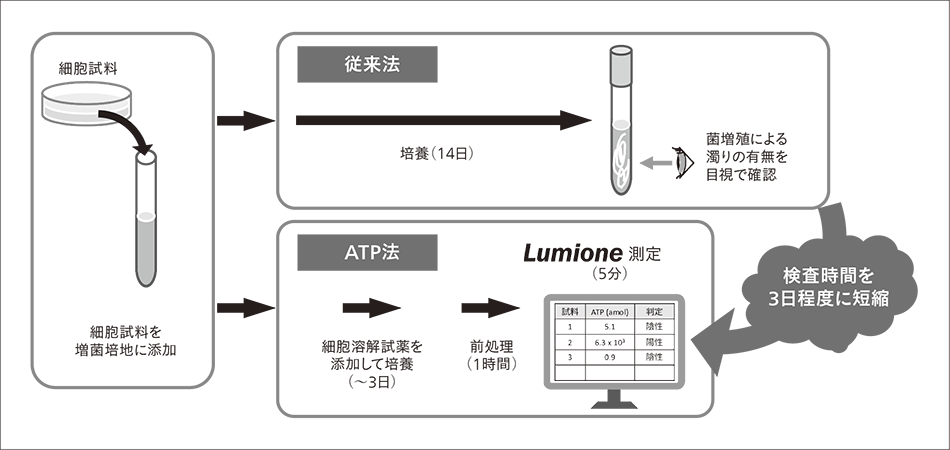
細胞製剤は生細胞を含むために最終製品の滅菌ができないという性質上,製造は全工程が無菌操作で行われ,最終製品に無菌試験が実施される。無菌試験手順の一例を図3に示す。
細胞を含む試料では,細胞が検査を阻害するという問題がある。従来法では,試料中に細胞が存在すると細胞自体によって培地に濁りが生じ,目視判定の妨げとなる。また,ATP法の場合は細胞自体が持つATPが菌検出を阻害する。例えば試料中に細胞が107個程度ある場合,この細胞が持つATPは細菌108個のATP量と同程度なので,細菌を108個まで増菌培養しても菌を検出することはできない。また,細胞のサイズは菌と同等かそれより大きいため,フィルタ濾過で細胞を除去することはできない。
日立はこの問題を解決する技術として,細胞のみを選択的に溶解してフィルタ濾過による除去を可能とし,なおかつ菌の増殖を阻害しないという性質を持った細胞溶解試薬を開発し,ATP法による迅速な菌検出を実現した。必要な培養時間は,細胞由来ATPの残量から決定される菌検出閾値,菌のATP内包量および増殖速度から決定される。
細胞溶解試薬を用い,細胞試料中から菌検出を行った例を図4に示す。免疫細胞治療や遺伝子細胞治療に用いられるヒトT細胞製剤を想定し,ヒト白血病T細胞由来の細胞株Jurkatを試料として用いた。Jurkat細胞107個/mLの懸濁液1 mL(溶媒:ジメチルスルホキシド10%,ウシ胎児血清5%含有リンゲル液)に,モデル菌株として,C. acnes 30 CFU,および無菌試験手法の適合性試験菌株のうち真菌であるAspergillus brasiliensis(A. brasiliensis:クロコウジカビ,ATCC 16404)25 CFUを添加し,局方に従いC. acnesは35℃,A. brasiliensisは25℃で,細胞溶解試薬の存在下で培養した。Jurkat細胞由来のATPは,試験開始直後はおよそ107 amolであった。これが,細胞溶解試薬の作用で時間とともに減少し,72時間後では10 amol程度と,6桁低減させる効果があった。温度が高い方が減少は速い傾向が見られたものの,培養48時間後にはいずれの菌でも,菌を添加した細胞試料と無菌の細胞試料の間でATP量に10倍以上の差が見られ,菌を検出できた。細胞の状態や菌増殖のばらつきを考慮し,72時間程度で無菌判定可能と考えられる。
現在,1日以内で結果が得られる細胞試料の迅速無菌試験法の確立をめざして,より細胞除去効果の高い細胞溶解試薬を開発中である。他の細胞種や菌種についてもデータを蓄積して実用化を進めていく。
図4|細胞試料からの菌検出の測定例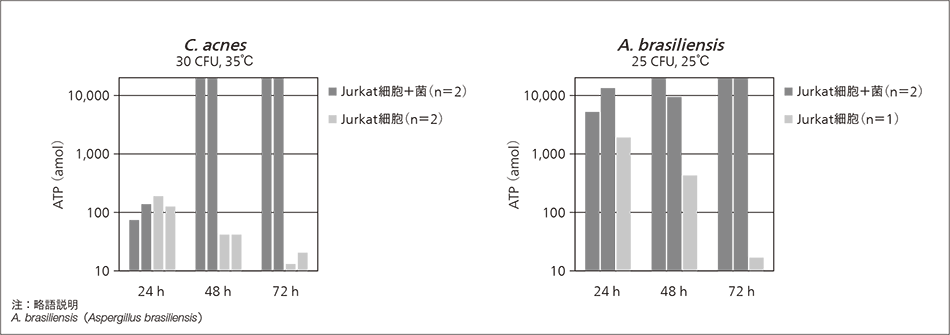 細胞溶解試薬を添加することにより,Jurkat細胞由来のATPは時間とともに減少した。一方,菌は増殖しATPは増加した。培養48時間後には,C. acnes,A. brasiliensisでともに,菌を添加した細胞試料と無菌の細胞試料の間でATP量に10倍以上の差が見られ,菌検出が可能であった。
細胞溶解試薬を添加することにより,Jurkat細胞由来のATPは時間とともに減少した。一方,菌は増殖しATPは増加した。培養48時間後には,C. acnes,A. brasiliensisでともに,菌を添加した細胞試料と無菌の細胞試料の間でATP量に10倍以上の差が見られ,菌検出が可能であった。
5. おわりに
日立はATP法により菌を高感度検出する微生物迅速検査装置Lumioneを開発し,医薬品製造における微生物検査の迅速化,医薬品の品質管理の向上に貢献している。今までに,製薬用水検査,低分子・高分子医薬品の無菌試験に加え,環境検査,細胞製剤の無菌試験への適用を検討してきた。
今後は,原料や工程内の微生物検査の迅速化をめざした技術開発,および顧客協創による製造現場のニーズに即した検査法への改良および実用化を進めていく。また,開発した技術を化粧品や食品といった分野に展開し,幅広く製造現場での微生物管理の向上に寄与していく。
参考文献など
- 1)
- 厚生労働省,第十七改正日本薬局方(2016.3)
- 2)
- 佐々木次雄,外:新GMP微生物試験法 第3版,じほう(2016.9)
- 3)
- 栗山伸一,外:再生医療等製品の微生物試験の現状と課題,日本防菌防黴学会誌,vol. 49,No. 12,pp. 641~645(2021.12)
- 4)
- 独立行政法人医薬品医療機器総合機構,再生医療等製品の無菌製造法に関する指針(2019.11)(PDF形式、514kバイト)
- 5)
- 福薗真一,外:医薬品の品質を担保する微生物迅速検査装置Lumione BL-2000,日立評論,100,6,654~661(2018.11)